郑州华赞医药科技有限公司
联系人: 刘经理电话: 0371-55023483
手机: 150-3805-1091
传真: 0371-55023483
邮箱: huazanchem@126.com
地址: 郑州市中原区中原西路131号49号楼12层1204号

央视焦点访谈:新药审批进入快车道
由于药品审评审批制度的原因,导致新药在中国上市很慢,但随着《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》的出台,以及CFDA加入ICH,国内外临床数据互认、临床机构资格改为备案制、增加药审人员数量、临床试验由明示许可改为默示许可等等措施,我国新药上市的速度将大大提升。这不,9价HPV疫苗从企...
多年来,新药在中国上市很慢,一些国外的好药迟迟难以进入中国市场,可是患者的病情不能等,救命不能等,有的患者不得不托人到海外购买药品,有的代购者还因此被判刑。为什么新药上市慢?关键在于药品审评审批的速度慢。
去年,中办、国办联合发布了《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,这对老百姓用药会带来什么影响呢?
海外代购药品是近年来兴起的一种现象。在QQ上输入“丙肝”二字,就能找到很多代购治疗丙肝药物的群,有的直接标明印度直邮、新药代购等字样。对于一些丙肝患者来说,到海外代购药品已经好几年了。
前几年在美国上市的一种新药,由于治愈率比较高,被称为治愈丙肝的神药,一个疗程的药品在美国的售价高达8万美元。不仅贵,直到2017年9月前,这种药还不能进入中国市场,而同样剂量的药通过网络代购印度的仿制药只需要900美元,一些患者就选择通过这样的灰色渠道购药。
因为销售海外代购的药物是违法的,在有的地方出现过因为销售代购药物被判刑的案例。但是患者对新药的需求却是刚性的。以一些肺癌患者为例,在服用一二代肺癌靶向药产生耐药性后,产自欧洲的第三代抗癌药就成为他们的救命药。
这种药在中国上市前,从上市较早的国家代购就成了不得已的选择,而有的患者甚至不顾风险根据公开的配方,通过互联网找到一些药粉,配上淀粉用天平称重量,放在胶囊里面服用。
某海外药品代购告诉记者:“这种药没有经过任何的临床试验,患者冒着生命危险,不得不去吃这种原料药。”
为了吃上新药,一些大病患者可谓冒尽风险、吃尽苦头。我国市场上的新药、疫苗、医疗器械上市时间大都落后于欧美,这其中最广为人知的就是宫颈癌疫苗,它在国外上市近10年之后,在我国才获准上市。
根据我国药监部门提供的数据,2001至2016年发达国家批准上市的433种新药,在中国上市的只有133种。近10年在我国上市的29个典型新药,上市时间也比欧美晚5至7年。

中国医药创新促进会执行会长宋瑞霖认为:“中国在药品的监管领域没有和国际完全对接,没有进行国际互认。你(国外药企)的临床数据不能直接应用于在中国的申报,这是两个国家,两种制度,我们更多把它看成了一种管理权的分割,而没有通过这个权力,看到背后我们追求的目标是为了患者的利益。”
国内外临床数据不互认,是导致上市慢的一个重要原因,除此以外,临床试验机构少、审批机构专业人员少、审批流程不合理等原因导致我国药品医疗器械发展速度满足不了公众用药的需求。
我国药监部门发布的《2015年度药品审评报告》显示,约120名药审中心工作人员完成了2015年9601件审评任务,但仍然有1.7万件积压。国内一些医药企业说到新药审批都很头疼。
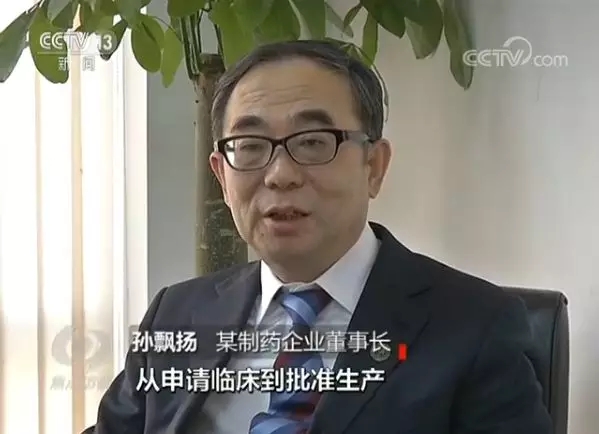
某制药企业董事长孙飘扬告诉记者:“我们从2001年做的第一个新药是治疗骨关节炎,这个新药研发从申请临床,到批准生产,花了10年左右的时间。其中一半时间是花在审批过程中,只有一半或者一半不到的时间用在临床试验,所以这10年时间大部分都被耽搁在审批上了。”
医药和器械审批慢,新药上市就慢,严重影响了老百姓用药和治疗,改革势在必行。在中办、国办联合发布的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》中第一条就提出将临床试验机构改为备案管理。临床试验是医药审批审评的关键环节。
过去,通过认定的临床试验机构仅600余家,能够开展Ⅰ期临床试验的机构仅有100余家。目前,全国现有各级医疗机构98.9万家,其中三级医院2万多家(编辑注:此处数据有误,据国家卫健委数据显示,截止至2018年2月,我国共有医院3.1万家,其中公立医院1.2万家,显然三级医院不可能有2万家。)。从资格认定改成备案管理,意味着符合条件的医疗机构都可能成为临床试验机构。
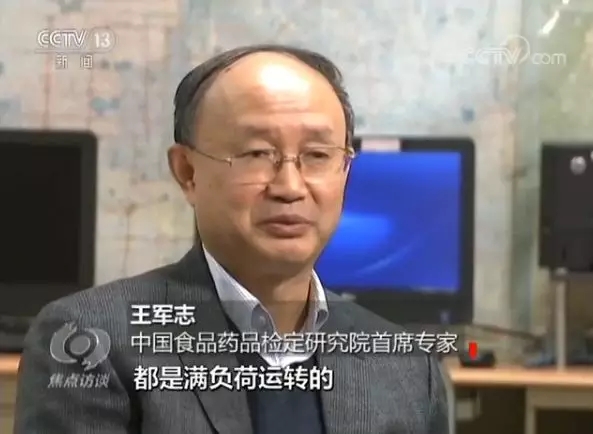
中国食品药品检定研究院首席专家王军志说:“所有的临床基地承担临床试验的都是满负荷运转的,包括医疗器械包括药品,上了临床以后都要做临床试验,这个资源现在是不够了。这次改革以后,一方面调动临床大夫和临床医院,承担国家创新药的临床评价积极性。实际上最后的结果还是老百姓受益,让老百姓更快获得创新药。”
一方面扩大临床试验机构的数量,另一方面,在《意见》中,明确提出接受企业在境外取得的临床试验数据。有条件地接受临床试验数据是加快药物在中国上市的迫切需要,也是中国医药产业与国际接轨的需要。
2017年6月,我国药监部门成为国际人用药品注册技术协调会(ICH)的成员,ICH的一个重要目标就是协调国际药品注册标准。这一行动被看作是中国药品监管向国际标准看齐的标志性事件。
据了解,在两年多以前,药品医疗监管体制已经开始了改革。2015年8月,国务院印发《国务院关于改革药品医疗器械审评审批制度的意见》,对这一领域进行了一系列变革。
药品审评中心工作人员从5年前的100余人增加到600多人。以此为基础,这次两办发布的《意见》总结了近年来改革的实践经验,提出了进一步优化药品上市程序的措施。比如,在申请人事先沟通基础上,将临床试验由明示许可改为默示许可。

从明示许可改为默示许可,一字之差,不仅会大大加快审批速度,而且代表着监管思路的重大变化。

“产品质量、药品质量不是监管出来的,是生产出来的,如果生产者抱着一个不正确的心态,去规避监管,那你的产品一定有巨大的风险。”宋瑞霖认为:“所以现在政府部门改革思路,把过于多的前置性的审批,把重心放到过程的监管,这是非常正确的,而且这也是在国际经验上我们论证是非常成功的一个范例。”
现在,为了加速一些用于治疗危重疾病的药品审评,我国药监部门设立了快速通道、优先审评、加速审批、突破性疗法等4条特别审批通道。

2017年10月19日,我国药监部门批准了“重组埃博拉病毒病疫苗”的新药注册申请。这是由我国独立研发、具有完全自主知识产权的创新性重组疫苗产品,为我国在埃博拉病毒爆发时有效控制疫情提供保障。据了解,2015年研制企业提出申请,2017年4月该品种正式申报生产注册,药监部门随即将该申请纳入优先审评程序,10月下旬获得批准。
埃博拉疫苗的上市,标志着我国药品有条件批准的开端。在这次两办发布的《意见》中,对这一点有了进一步的明确。《意见》中提到,“对治疗严重危及生命且尚无有效治疗手段疾病,以及公共卫生方面等急需的药品医疗器械,临床试验早期、中期指标显示疗效并可预测其临床价值的,可附带条件批准上市。”
这样一个改变,对那些身患大病苦苦等待新药的病患来说有着特别的意义。2017年9月,节目开头提到的国外治疗丙肝的特效药已经在中国正式上市,这是中国患者和医生都期盼了很久的事情,可是要让患者真正感受到改革的利好,尽快用上新药,这只是第一步。
由于新药价格昂贵,还是让很多人望而却步。据医生介绍,同样成分疗效的药,合法进口到中国的价格多在五六万元以上,是到印度代购仿制药的三四倍以上,所以患者难以承受,还是只能选择非法渠道。

要解决这一问题,这就涉及到相关机构的综合统筹,在《意见》中,我们也看到了这一改革目标。《意见》中要求,要“完善医疗保险药品目录动态调整机制,探索建立医疗保险药品支付标准谈判机制,及时按规定将新药纳入基本医疗保险支付范围,支持新药研发。各地可根据疾病防治需要,及时将新药纳入公立医院药品集中采购范围。”

北京友谊医院肝病中心主任贾继东表示:“尽管晚了一些,这一天还是来了,我们觉得很高兴。但是如果价格高高在上,又不能及时纳入医保或者各种报销的体系,患者还是不能真正享受到改革加快审批带来的红利。希望政府、各个部门之间能够加强协调,通过国家谈判,能够争取到一个很好的、很低的价格,这样药厂能赚到钱,同时医保也能承担得起。”

药品审评审批的提速不仅对老百姓来说是个好消息,对中国的药企来说,这也是一个大利好,有助于药企增加研发投入、释放创新潜力、提升创新能力,最终促进医药产业的发展,惠及所有民众。